편집자 주
월요일 아침, 지하철이나 버스를 타본 경험 있으신가요? 한 번쯤은 ‘왜 유독 월요일엔 사람이 더 많지?’ 하고 궁금했던 적도 있었을 겁니다. 매일 같은 시간, 같은 경로를 이용하지만, 요일에 따라 붐빔의 정도는 다르게 느껴집니다. 이처럼 우리는 일상 속에서도 반복되는 패턴과 규칙을 발견하곤 합니다. 그리고 그 이유가 궁금해질 때가 있죠. 때로는 그런 호기심이 새로운 발견의 출발점이 됩니다.

오래전부터 많은 과학자들은 원소들을 분류하거나 일정한 기준에 따라 배열하려는 시도를 계속해 왔습니다. 예를 들어, 독일의 화학자 요한 볼프강 되베라이너는 화학적 성질이 비슷한 세 원소들을 관찰하던 중, 원자량이 가장 큰 원소와 가장 작은 원소의 평균이 나머지 한 원소의 원자량과 매우 비슷하다는 사실을 발견했습니다. 리튬(Li), 나트륨(Na), 칼륨(K), 모두 반응성이 크고 물과 격렬하게 반응하는 공통된 성질의 세 원소들을 본다고 할 때, 리튬의 원자량은 약 7, 칼륨은 약 39이며, 나트륨의 원자량은 이 둘의 평균값인 약 23과 매우 유사한 22.99였습니다.
되베라이너는 이런 관계를 갖는 원소 무리를 ‘세 쌍 원소(Triads)’라 명명하고, 원소들 사이에도 일정한 패턴이 존재할 수 있다는 가능성을 제시했습니다. 이후 여러 과학자들이 원소의 성질과 배열 사이의 규칙을 찾기 위한 노력을 이어갔습니다. 1860년대, 영국의 화학자 존 뉴랜즈는 원소들을 원자량 순으로 나열 했을 때, 여덟 번째마다 성질이 비슷한 원소가 반복된다는 사실을 발견했습니다. 그는 이 규칙을 음계에 빗대 ‘옥타브 법칙’이라 불렀지만, 당시 과학계의 주목을 받지는 못했습니다.
그로부터 얼마 지나지 않아, 러시아의 화학자 드미트리 멘델레예프는 원소들을 원자량 순으로 배열하면서 성질이 비슷한 원소 들이 주기적으로 나타나는 패턴을 보다 체계적으로 정리해 나갔습니다. 그는 자신이 만든 표에서 아직 발견되지 않은 원소들의 자리를 비워두고 그 성질과 원자량까지 예측했습니다.
|
김태영 쌤의 통합과학,
이것만은 꼭!
통합과학에서는 같은 족의 원소들끼리 유사한 화학적 성질을 가진다는 것을 설명하기 위해 1족 원소인 알칼리 금속과 17족 원소인 할로젠 원소를 예로 들어 설명합니다. 특히 알칼리 금속이나 할로젠 원소의 유사성을 탐구하는 실험 자료가 교과서에 실려 있으므로 이를 정확하게 알고 있는 것이 중요합니다.
|
 |
| 구분 | 알칼리 금속 | 할로젠 원소 |
|---|---|---|
| 족 |
|
|
| 금속/비금속 |
|
|
| 실온에서 상태 |
|
|
| 물리 법칙 |
|
|
이후 그 예측에 들어맞는 원소들이 발견되면서 멘델레예프의 주기율표는 큰 주목을 받습니다. 그러나 여기엔 아직 예외와 오차들이 남아 있었죠. 이 문제를 해결한 인물이 바로 영국의 물리학자 헨리 모즐리입니다. 그는 원소의 속성을 결정하는 핵심이 원자량이 아니라, ‘원자번호(양성자수)’라고 주장합니다. 그에 따라 주기율표의 배열 기준이 정립되면서 현재 우리가 이용하는 현대적인 주기율표 형태가 완성돼 왔습니다. 주기율표의 가로 줄을 ‘주기’라고 하며, 같은 주기에 해당하는 원소들은 갖고 있는 전자껍질 수도 같습니다. 주기율표의 세로 줄은 ‘족’이라고 하며, 같은 족 원소들은 화학적으로 성질이 비슷합니다. 이는 원자를 구성하는 전자의 배치와 관련이 깊습니다.
보어가 제시한 원자 모형에 따르면, 원자핵 주변을 도는 전자들은 특정한 에너지 준위를 가지며, 정해진 원형 궤도, 즉 전자껍질을 따라 운동합니다. 이러한 전자껍질은 핵에서부터의 거리와 에너지 수준에 따라 구분되며, 각 껍질에는 들어갈 수 있는 전자의 수가 정해져 있습니다. 일반적으로 원자핵에 가장 가까운 첫 번째 껍질에는 최대 2개, 그 바깥쪽 두 번째 껍질에는 최대 8개, 그 다음 세 번째 껍질에는 최대 18개의 전자가 들어갈 수 있습니다.
원소의 가장 바깥 전자껍질에 들어 있으면서 화학 결합에 참여하는 전자들을 우리는 ‘원자가 전자’라고 합니다. 원자가 전자는 화학 결합에 관여하므로 원소의 화학적 성질을 결정하는 중요한 요소입니다. 대부분의 원자들은 전자껍질이 전자로 완전히 채워진 안정된 상태를 선호합니다. 예를 들어 원자번호 3번인 리튬(Li)은 첫 번째 껍질에 전자 2개가 채워지고, 두 번째 껍질에 나머지 1개의 전자가 있습니다. 리튬이 두 번째 껍질을 전자 8개로 가득 채우려면 전자 7개를 더 얻어야 하지만, 그보다는 전자 1개를 잃고 첫 번째 껍질만 채운 안정된 상태가 되는 게 훨씬 쉬운 선택입니다. 따라서 리튬은 전자를 하나 잃고 리튬 이온(Li+)이 되려고 합니다.

이런 성질은 원자가 전자가 1개인 다른 1족 원소들에서도 공통적으로 나타납니다. 1족 원소에서 비금속 원소인 수소(H)를 제외한, 나머지 리튬(Li), 나트륨(Na), 칼륨(K), 루비듐(Rb) 등을 알칼리 금속이라고 합니다. 알칼리 금속 은 원자가 전자가 1개이므로 전자 1개를 잃어 양이온이 되기 쉬우며, 이온 결합이 쉽게 일어납니다. 나트륨(Na)이 물(H2O)과 반응하면 나트륨 이온(Na+)과 수산화 이온(OH-)이 이온 결합을 하고, 수소 기체(H2)가 생성됩니다.
반대로 1개의 전자를 쉽게 얻어서 안정된 상태가 되려는 원소들도 존재합니다. 17족 원소들, 플루오린(F), 염소(Cl), 브로민(Br), 아이오딘(I) 등은 가장 바깥쪽 전자껍질에 7개의 전자를 가집니다. 즉, 1개의 전자를 더 얻으면 전자껍질을 완전히 채워 안정한 전자 배치를 갖게 됩니다. 이러한 17족 원소들을 할로젠 원소라고 하며, 할로젠 원소들은 실온에서 2개의 원자가 결합한 분자, 즉 이원자 분자 형태로 존재합니다. 부족한 1개의 전자를 다른 원소로부터 얻는 대신, 같은 할로젠 원자끼리 전자 1개씩을 공유해 서로의 껍질을 채운 거죠. 물론 다른 원자로부터 전자를 받기도 합니다. 전자를 하나 잃기 쉬운 알칼리 금속과 할로젠 원소가 반응하면, 알칼리 금속이 잃은 전자를 할로젠 원소가 받을 수 있습니다. 이 경우 전자를 잃은 알칼리 금속 이온(M+)이 전자를 얻은 할로젠 음이온(X-)과 이온 결합을 할 수 있습니다.
이처럼 원자가 전자의 분포와 그로 인한 결합 경향성은 원소의 반응성 뿐만 아니라 물질이 형성되는 방식, 나아가 생명체 구성 원리와도 연결됩니다. 지구를 이루는 암석은 주기율표 속 원소들이 다양한 결합을 통해 형성한 구조물이고, 생명체를 구성하는 DNA, 단백질 역시 특정한 전자 배치와 결합 성향을 바탕으로 정교하게 조직돼 있습니다. 주기율표가 지구 환경과 생명 현상,원자의 구조를 설명하는 물리적 원리까지 모두 포괄하고 있는 셈입니다.
김태영
통합과학 개념 실전 탐구

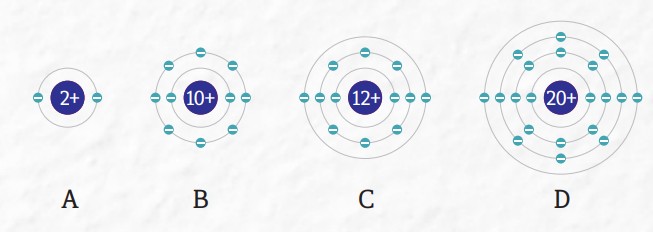
Q.원자 A~D의전자 배치를 모형으로 나타낸그림이다. A~D에대한 설명으로 옳은 것은 ‘O’, 옳지않은 것은 ‘X’로 표시해보자.
②A와 B는 모두 비금속이다.(○, ×)
③B와 C는 같은 주기의 원소다.(○, ×)
④C와 D의 화학적 성질이 유사하다.(○, ×)
A.×, ○, ×, ○
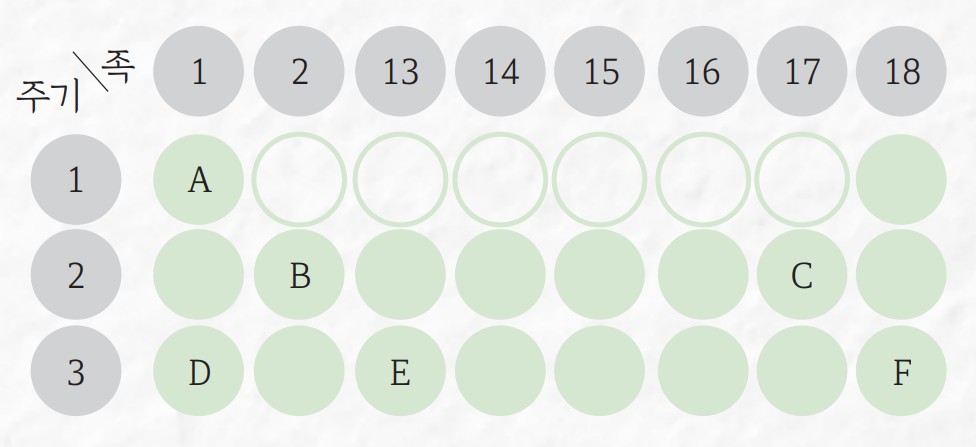
Q.주기율표의일부를 나타낸그림이다. A~F는 임의의원소다. A~F에대한 설명으로 옳은 것은 ‘O’, 옳지않은 것은 ‘X’로 표시해보자.
②A~F 중 원자가 전자 수가 가장 큰 원소는 F다.(○, ×)
③A와 C가 반응해 생성된 화합물은 물에 녹아 산성을 나타낸다.(○, ×)
④D는 실온에서 은백색 광택을 띠는 고체상태다.(○, ×)
A.×, ×, ○, ○
(2) F의 가장 바깥쪽 전자 껍질에 있는 전자 수는 8개이지만, 이 전자들은 다른 원소와 잘 반응하지 않으므로 F의 원자가 전자 수는 0이다. 따라서 A~F 중 원자가 전자의 수가 가장 큰 원소는 C이며, C의 원자가 전자 수는 7이다.
(3) A(H)와 C(F)가 반응하여 생성된 화합물 HF는 물에 녹아 산성을 나타낸다.
(4) D(Na)은 알칼리 금속으로 실온에서 은백색 광택을 띠는 고체 상태이다.

①[탄생 150주년] 알아두면 쓸모있는 신기한 주기율표 이야기(기사클릭)
과학동아 2019년 4월호
“엄밀히말해주기율표는 아직완성되지 않았다. ‘완벽한 주기율표’ 제작은 여전히 현재진행형이다.”
해설: 주기율표는 새로운 원소가 발견되거나 화학적 성질에 대한 이해가 깊어질수록 계속해서 변화할 수 있습니다. 오늘날 다양한 형태의 주기율표가 존재하며, 이를 통해 주기율표는 여전히 진화하는 과학의 산물임을 알 수 있습니다.
②볼풀과 원자모델 푸딩, 복숭아 그리고 다음은?(기사클릭)
과학동아 2006년 6월호
“양자역학의중심에는 두 가지중요한 개념이있다. 하나는, ‘원자와 같이 아주 작은 세계에서는 많은 성질이 불연속적’이라는 것이다.”
해설: 보어는 전자가 아무 궤도에나 존재하는 것이 아니라, 특정한 에너지준위를 가지는 궤도에만 존재할 수 있다고 제안했습니다. 이러한 관점은 물리학의 양자 개념과 화학의 원자 구조 이론을 연결짓는 중요한 이정표가 됐습니다.
③소금은 분자일까? 아닐까?(기사클릭)
과학동아 2006년 9월호
“나트륨(소듐)은 원자 세계의 전자 기부자다. 하지만 나트륨이 전자 하나를 잃고 더 안정한 나트륨이 된다는 생각은 오해다.”
해설: 기사를 통해이온 결합이 형성되는 원리와 ‘분자’의 개념에 대해 이해할 수 있습니다. 이온 결합물은 개별 분자로 존재하는 것이 아니라 규칙적인 배열을 이루는 결정 구조로 존재하기 때문에, 일반적으로 사용하는 ‘분자’의 정의와는 다릅니다
















(1) A의 원자가 전자 수는 0, C의 원자가 전자 수는 2이다.
(2) A와 B는 비금속, C와 D는 금속 원소이다.
(3) 주기는 전자가 들어 있는 전자 껍질 수에 의해 결정된다. B는 2주기 원소이고, C는 3주기 원소이다.
(4) C와 D는 모두 2족 원소이며, 원자가 전자 수가 2로 같으므로 화학적 성질이 유사하다.